


記事と筆者の信頼性
・難関大学に化学受験で合格した人が記事を執筆
・早稲田大学卒の予備校講師が、さらに分かりやすく編集
・編集者は予備校講師として、2,000人以上の受験生を指導
無機化学における金属の沈殿は、大学入試の化学の試験で頻出のテーマです。
特に理系学部志望の受験生であれば、難関大学に限らず、どの大学でもほぼ確実に出題されるでしょう。
大学入学共通テストでも、もちろん沈殿に関する問題が出題される可能性があります。
そんな無機化学分野の沈殿について解説していきます。

>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
目次
無機化学は丸暗記で乗り越えられるの?

無機化学を苦手とする受験生に多いのが「暗記事項が多くて覚えきれない」という声。
確かに無機化学の分野は、理論化学の分野と比べると暗記の色が強い分野であることは間違いありません。
しかし「暗記だけで点が取れるか?」というと全くそうではありません。
ただでさえ覚えなければならないことが山積みの大学受験おいて、単純な暗記作業にのみ頼っていては、絶対に点数は上がりません。
しっかり覚えるべきところと、理解しながら勉強する部分をメリハリをつけて進めていきましょう。
重要なポイントをまずは固めよう

勉強の指針としては「教科書レベルの内容は確実に抑えて、資料集などの細かい部分は後回しにする」ことを意識してください。
試験に頻出の教科書に記載のある、必須事項に絞って紹介していきます。
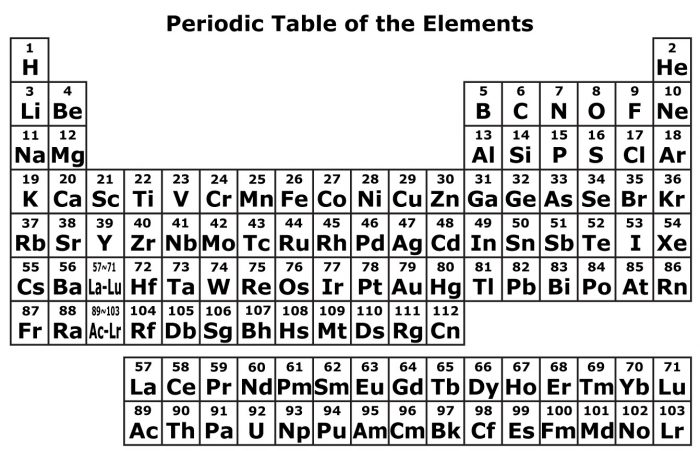
引用元(化学の迷路)2020/03/09
基本的に沈殿するものを中心に覚えていくことがコツ。
それ以外は「例外を除いて沈殿しない」という考え方で問題ありません。
割り切って整理していくことで、効率的に暗記をできるようになります。

>>1ヶ月で早稲田慶應・難関国公立の英語長文がスラスラ読めるようになる方法はこちら
塩化物イオン(Cl-)で沈殿する金属イオン
塩化物イオンで沈殿する金属イオンのうち、覚えるべきものは
Pb2+(鉛イオン)とAg+(銀イオン)のたった2つです。
【ゴロ合わせ】演歌の訛り(なまり)ギンギン
演歌(塩化物イオン)の訛り(Pb)ギンギン(Ag)
沈殿の色はすべて白色
両者を区別する方法は加熱することで、
AgClは変化しない
PbCl2溶ける(無色溶液になる)
ここはAgClとPbCl2の沈殿を判別する唯一の方法なので、絶対に押さえておきましょう。
硫酸イオン(SO42-)で沈殿する金属イオン
硫酸イオンで沈殿する金属イオンのうち、覚えるべきは
Ba2+(バリウムイオン)、Ca2+(カルシウムイオン)、Pb2+(鉛イオン)です。
【ゴロ合わせ】バカなりゅうさん
バ(Ba) カ(Ca) な(Pb)りゅうさん(硫酸イオン)
沈殿の色はすべて白色
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
炭酸イオン(CO32-)による沈殿
炭酸イオンで沈殿する金属イオンは、硫酸イオンで沈殿する金属イオンと重複しています。
【ゴロ合わせ】たくさんのバカ
たくさん(炭酸イオン)のバ(Ba) カ(Ca)
沈殿の色はすべて白色
クロム酸イオン(CrO₄²⁻)で沈殿するイオン
ここまで扱った陰イオンと金属イオンの沈殿は、すべて白色でした。
ここで扱うクロム酸イオンと金属イオンの沈殿は、カラフルですので印象に残りやすいかもしれません。
ここで覚えるべき金属イオンは、Ba2+(バリウムイオン)、Pb2+(鉛イオン)、Ag+(銀イオン)の3つです。
【ゴロ合わせ】菜畑で銀貨落として苦労した
菜(Pb)畑(Ba)で銀(Ag)貨落として苦労(クロム酸イオン)した
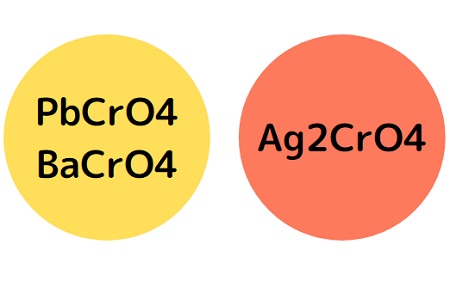
沈殿の色は
PbCrO4は黄色
BaCrO4は黄色
Ag2CrO4は赤褐色
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
硫化物イオン(S²⁻)で沈殿するイオン
ここからは、水溶液のpHによって沈殿したり、しなかったりとややこしくなってきます。
ここを苦手とする受験生はかなり多いでしょう。
難関大学でも狙われやすい部分です。
しっかり固めておけば、試験本番で周りと差をつけることができます。
イオン化傾向の復習

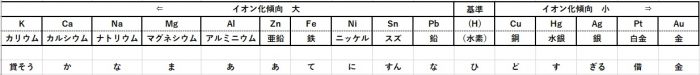
上のように、有名なゴロと一緒に覚えるのが効果的。
このイオン化傾向の表を踏まえたうえで勉強すると、効率的に勉強を進められます。
中性・塩基性の溶液でのみ沈殿するイオン
中性・塩基性の溶液でのみ沈殿するイオンは

Zn2+、Fe2+(Fe3+も)、Ni2+
沈殿の色は
ZnSは白色
FeSは黒色
NiSは黒色

>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
溶液がどんなpHでも沈殿するイオン
溶液がどんなpHでも(酸性・中性・塩基性すべてにおいて)沈殿するイオンは

Sn2+、Pb2+、Cu2+、Hg2+、Ag+
沈殿の色は
SnSは褐色
PbSは黒色
CuSは黒色
HgSは黒色
Ag2Sは黒色
ここまでの内容を軽く復習!

最後にもう一度、中性・塩基性の溶液でのみ沈殿するイオンと
溶液がどんなpHでも(酸性・中性・塩基性すべてにおいて)沈殿するイオン
を沈殿の色にも注目しながら表で見ると、下の通り。

つまり、基本的に硫化物イオンの沈殿は黒色。
それ以外の色を呈する沈殿に気をつければ、より勉強がしやすいでしょう。
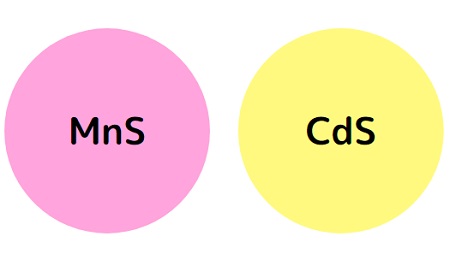
他に、硫化物イオンの沈殿で有名なのは、
MnS (中性・塩基性の溶液でのみ沈殿する)は淡桃色
CdS(溶液がどんなpHでも(酸性・中性・塩基性すべてにおいて)沈殿する)は黄色
>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
塩基によって沈殿するイオン
最後は塩基(水酸化ナトリウム水溶液やアンモニア水)との反応によって生じる、水酸化物の沈殿です。
量が多いように感じますが、下の表を見つつ、ポイントを押さえれば分かりやすいでしょう。
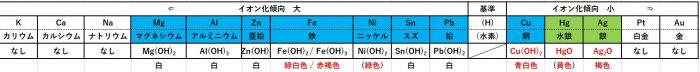
暗記の際のポイント

水酸化物の沈殿で例外は2つ
Hg2+とAg+は、塩基(水酸化ナトリウム水溶液やアンモニア水)と反応すると、酸化物の沈殿を生じます。
水酸化物の沈殿は、基本的には白色
下の例外のものを中心に、しっかり覚えましょう。
Fe(OH)2 の緑白色
Fe(OH)3の赤褐色
Ni(OH)2の緑色
Cu(OH)2の青白色
HgOの黄色
Ag2Oの褐色
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
過剰なNaOH溶液を加えた場合
Al(OH)3、Zn(OH)2、Sn(OH)2 、Pb(OH)2の沈殿は溶けます(無色透明の溶液になる)。
【ゴロ合わせ】ああすんなり溶ける
あ(Al)あ(Zn)すん(Sn)なり(Pb)溶ける
過剰なNH3溶液を加えた場合
Zn(OH)2 、Cu(OH)2 、Ag2O の沈殿はすべて溶けます。
加えて、それぞれの溶液の色は
Zn(OH)2 無色透明の溶液
Cu(OH)2 深青色の溶液
Ag2O 無色透明の溶液
基本的に過剰なNaOH溶液、あるいは過剰なNH3溶液を加えて、沈殿が溶けた後の溶液の色は、無色透明です。
例外として、Cu(OH)2が溶けた後の溶液が深青色と覚えましょう。
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
実際に出題される沈殿の問題

ここまで学んだことを踏まえて、実際の問題で知識を確認してみましょう。
無機化学の分野はどうしても、暗記の時間が多くなってしまいます。
「全部の知識が完璧になってからやろう。」と、問題演習を後回しにする受験生も多いです。
しかし暗記事項が多い分野だからこそ、適度に問題演習を組み込むことをおすすめします。
問題演習をすることで知識の整理につながり、何よりミスをすることで自分の知識の抜けに気づくことができますからね。
それでは、何題か解いてみましょう。
(太字は問題を解く上でポイントになるヒントです。)
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
問題①
水酸化鉄(Ⅲ)Fe(OH)3と水酸化アルミニウム AI(OH)3の沈殿の混合物がある。
この混合物に過剰の水酸化ナトリウム水溶液を加えてろ過したとき、ろ紙上に残る沈殿とその色、ろ液の色を答えよ。
問題②
K+、Ca2+、Al3+、Cu2+ の4種類の金属イオンを含む混合水溶液に、次の操作①~④を行い、各イオンを分離した。
沈殿A~Cの化学式とその色、ろ液Dに含まれる金属イオンの名称を答えよ。
・酸性にして硫化水素 H2S を通じ、生じた沈殿Aをろ過で取り出した。
・①のろ液にアンモニア水 NH3 aq を加え、生じた沈殿Bをろ過で取り出した。
・②のろ液に炭酸アンモニウム(NH4)2CO3水溶液を加え、生じた沈殿Cをろ過で取り出した。
・③のろ液Dの炎色反応を調べると、赤紫色を呈した。
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
問題①の解説
まず問題文中に太字で示した「過剰の水酸化ナトリウム水溶液を加えて」の操作により、水酸化アルミニウム AI(OH)3の沈殿が溶けます。
その色は何色だったか覚えていたでしょうか?
答えは、無色透明です。
よって、ろ紙に残る沈殿は、水酸化鉄(Ⅲ)Fe(OH)3 となり、その色は赤褐色。
ちなみに水酸化鉄(Ⅱ)Fe(OH)2 の場合は、沈殿の色は緑白色です。
問題②の解説
操作が多いですが、順番に丁寧に見ていきましょう。
本番で時間に追われていると、ついつい条件を見逃してしまうことがありますので、注意してください。
操作①
操作①では、酸性の条件にしたうえで、硫化水素 H2Sを通じる、とあります。
この条件で沈殿を生成するのは、Cu2+です。
このことから、沈殿Aは、CuSとなり、沈殿の色は黒色となります。
操作②
操作②では、アンモニア水 NH3 aq を加えることで、溶液が塩基性になったと考えます。
塩基性の条件で沈殿を生じるのは、残りのK+、Ca2+、Al3+のうち、Al3+です。
よって、生成する沈殿BはAl(OH)3で、沈殿の色は白色となります。
操作③
操作③では、炭酸アンモニウム(NH4)2CO3水溶液を加えることで、炭酸イオンCO32-と、残った金属陽イオンの反応を考えます。
残っているのは、K+、Ca2+で、この中で炭酸イオンCO32-と反応するのは、Ca2+です。
よって生成する沈殿CはCaCO3で、沈殿の色は白色となります。
操作④
操作④は最終確認作業という意味合いです。
炎色反応が赤紫色ということから、ろ液Dに含まれる金属イオンはK+となります。
>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
無機化学分野はどんどん演習しよう
無機化学の分野は、演習を積めば積むほど、解くスピードはもちろん、精度も上げることができます。
問題を通して教科書には記載されていないような、発展的な新しい知識を身につけることもできるでしょう。
コツコツと演習した努力の積み重ねが、そのまま点数に還元される分野なので、積極的に問題演習をしてください。
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
演習におすすめの問題集
化学重要問題集

入試の標準~やや発展的なレベルの問題まで幅広く記載されています。
A問題とB問題に分かれていますが、基本的なA問題だけでも完璧にすれば、目に見えて成績が上がります。
関連記事
化学の新演習

入試の中でも、難問が多く記載されています。
ややオーバーワークになってしまうという人が多い問題集なので、理系難関大志望者や難関学部志望者の中で、化学を得点源にしたい人が使うと良いでしょう。
大学入試の過去問もおすすめ

大学入試の過去問は、合格者なら全問正解したい基礎問題から、やや難しい問題までバランス良く収録されています。
これらの大学の過去問演習をすることで、基礎~応用まで、実践的な問題を幅広く解くことができます。
自分が志望する大学の過去問はもちろんのこと、同じレベルの大学や併願校の過去問も解いておきましょう。
模試を積極的に受けて、より実践に近い形で演習をすることも、もちろん効果的です。
⇒1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら
現役の時に偏差値40ほど、日東駒専に全落ちした私。
しかし浪人して1ヶ月で「英語長文」を徹底的に攻略して、英語の偏差値が70を越え、早稲田大学に合格できました!
私の英語長文の読み方をぜひ「マネ」してみてください!
・1ヶ月で一気に英語の偏差値を伸ばしてみたい
・英語長文をスラスラ読めるようになりたい
・無料で勉強法を教わりたい
こんな思いがある人は、下のラインアカウントを追加してください!
筆者は現役時代、偏差値40ほどで日東駒専を含む12回の受験、全てに不合格。
原因は「英語長文が全く読めなかったこと」で、英語の大部分を失点してしまったから。
浪人をして英語長文の読み方を研究すると、1ヶ月で偏差値は70を超え、最終的に早稲田大学に合格。
「1ヶ月で英語長文がスラスラ読める方法」を指導中。
⇒【秘密のワザ】1ヵ月で英語の偏差値が40から70に伸びた方法はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら











